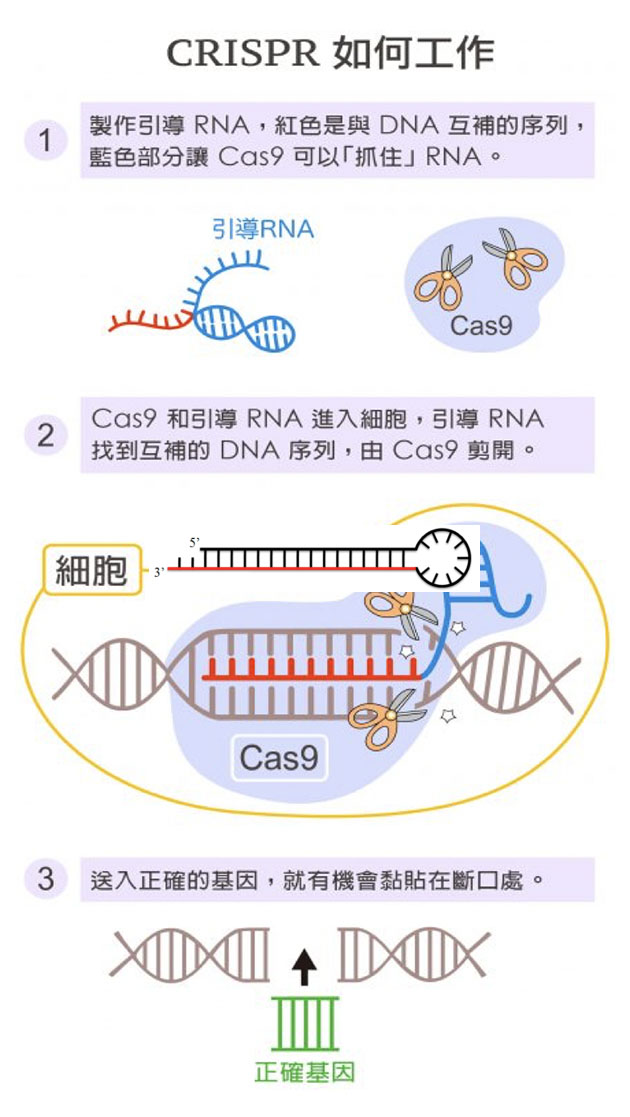
《題型解析》:幹細胞研究是再生醫學重要一環,此題純粹是送分,屬於簡單易寫的問題。此題容易拿下15-20分,甚至滿分25分。
誠如上課一再提醒,解釋名詞一定要詳細了解。抗體抗原特異性是細胞分離與免疫分析的關鍵,特異性抗體的親和性管柱與流式細胞分類儀(flow cytometry mrthod)加以分離純化,即可得分。最後是衛福部的細胞治療特管法。
誠如上課一再提醒,解釋名詞一定要詳細了解。抗體抗原特異性是細胞分離與免疫分析的關鍵,特異性抗體的親和性管柱與流式細胞分類儀(flow cytometry mrthod)加以分離純化,即可得分。最後是衛福部的細胞治療特管法。
- 幹細胞的定義與特性
幹細胞(stem cells)是生物體最原始未分化的細胞,它具有再生與分化的能力,可以增殖成為原來相同的細胞也可以分化成為其他細胞如肝細胞,肌肉細胞,血球細胞等,以及其他具有特定功能的細胞。簡言之,幹細胞係指一群尚未分化、但具有自我更新的能力、以及增殖分化成各類成熟組織能力的原始細胞。
幹細胞因具有以上這些特性,所以可用來修補受損的組織或器官,甚至還可以建構出完整的器官。幹細胞被稱為“源母全功能細胞”,因為它們具有形成特定的組織分化及或器官發育的能力。 - 胚胎幹細胞、成體幹細胞與誘導式多功能性幹細胞
- 胚胎幹細胞特性:
胚胎幹細胞(embryonic stem cell)存在於胚胎發育早期,受精卵分裂五天後囊胚中,可發育為不同的細胞,是所有細胞最初期的形態,能分化出成體的所有組織和器官,包括生殖細胞等。- 成體幹細胞特性:
成體幹細胞(adult stem cell)也稱成人幹細胞,存在於已成熟的個體的成體組織中,典型的代表包括骨髓幹細胞、脂肪幹細胞、造血幹細胞與間質幹細胞等,這些幹細胞並不是全能幹細胞,被稱之為多功能幹細胞。成體幹細胞的最佳例子是造血幹細胞。骨髓移植,幹細胞移植,或血液移植,被移植的細胞是造血幹細胞。這種細胞是主要存在於成人骨髓中。 - 誘導式多功能性幹細胞特性:
誘導性多能幹細胞(Induced pluripotent stem cell),又稱人工誘導多功能幹細胞,簡稱爲iPS細胞(iPSC),是一種由哺乳動物成體細胞經轉入特異分化轉錄因子等手段,可逆性分化形成的多功能幹細胞,最早由日本學者山中伸彌的研究團隊於2006年發現。山中伸彌團隊在發表iPS誘導技術時使用實驗材料爲小鼠成體細胞。2007年,研究人員又證明iPS誘導技術可以應用於人體細胞。最初由山中伸彌團隊發現的誘導方法是透過慢病毒載體將Oct4、Sox2、Klf4、c-Myc四種轉錄因子(OSKM被稱為山中因子)基因轉入成體細胞將其轉化爲類似於胚胎幹細胞的多能幹細胞。
人類的iPSC可以分化成為多種不同的胎兒細胞類型。iPS細胞在疾病發展和治療藥物的研究很有價值,並且它們可以具有在移植醫學未來用途上。
- 成體幹細胞特性:
- 胚胎幹細胞特性:
- 幹細胞之分離技術:
不同的幹細胞有不同的特異性表面抗原或分化標誌,因此,可用特異性抗體的親和性管柱 (affinity column) 與流式細胞分類儀(flow cytometer)加以分離純化。
以血液幹細胞的純化為例:它是利用一種新的血液幹細胞分離技術,來達到血液幹細胞純化的目的。- CD34是血液幹細胞的一種細胞分化標誌的表面抗原,絕大多數的血液惡性腫瘤細胞都不含此種抗原,因此,臨床上我們便可以透過利用此種表面抗原的細胞篩選技術來純化血液幹細胞。
- CD34血液幹細胞分離系統,目前臨床市面上常使用細胞純化機。此種臨床細胞分離系統(Clini MACS)是一種由永久磁鐵,一個蠕動推進幫浦及一組控制閥門所組成,由電腦控制的全自動操作機器,利用磁性分離細胞篩選技術的系統,在臨床上可以利用此分離技術作為CD34陽性細胞的分離並提供良好的細胞純度及活性。
- 在篩選過程中,乃是利用鼠抗人類CD34抗體與鐵菌葡萄聚糖分子共價結合的免疫磁珠,經過磁性標記後,系統自動將CD34陽性細胞留存於含有磁性的分離柱上,之後將磁力移除可使分離柱上脫離出被留存的細胞,再經過清洗即可完成CD34陽性細胞收集。
- 完整的細胞分離只須要3小時即可完成。
- 細胞治療的定義:
根據衛生福利部食品藥物管理署所定義的細胞治療:「使用取自病患同種自體、同種異體或異種異體或其他經中央主管機關核准之體細胞或幹細胞,並經體外培養後所衍生的細胞,以達到疾病治療、診斷或預防目的之醫療技術。」