志聖食品技師
106第二次食品分析與檢驗 試題詳解
| 擬答 6.25% = 6.25 mL/100 mL,所以4,000 L 含6.25% 為250 L/4000 L。 重量是1.02 Kg/L,所以250 L含玉米濃湯固形物重1.02 Kg x 250 = 255 Kg。 255 kg /X = 31.25%,所以 X = 816 Liter 為了達到標準固形物31.25%,需將4,000 L容積濃縮到816公升。 |
擬答
|
擬答
|
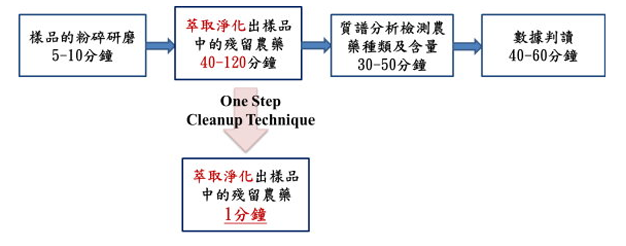
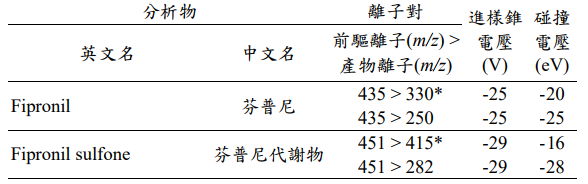
| 擬答 (此題在105-2食檢考過類似考題) 國際通用及公認最快速之農藥殘留萃取淨化技術為 QuEChERS (Quick、Easy、Cheap、Effective、Rugged and Safe)方法,衛福部食藥署公告之食品中殘留農藥檢驗方法-多重殘留分析法進行分析,使用檢測儀器為氣相層析串聯式質譜儀(GC/MS-MS)及液相層析串聯式質譜儀(LC/MS-MS),同時進行定量分析及藥劑確認。2012 年,此方法可同時分析藥劑種類約 251 種,但過程需要使用約 200 毫升的化學溶劑。衛福部食藥署持續研發「多種農藥殘留同時檢測技術」,開發多重殘留分析方法,由衛福部公告可同時檢驗 310 種農藥。 雞蛋檢體採用QuEChERS方法(Quick, Easy, Cheap, Effective, Rugged, Safe)前處理後,以液相層析串聯質譜儀(liquid chromatograph/tandem mass spectrometer, LC/MS/MS)分析之 方法。
|